Внедренные специалистами КриоЦентра методики, позволяют сохранить два вида биологических материалов, получаемых из ткани пупочного канатика (пуповины):
- выделенные мезенхимальные стромальные стволовые клетки (МСК) , которые при необходимости можно дополнительно размножать для последующего использования;
- собственно ткань пупочного канатика, которую, по истечении многих лет можно будет разморозить и использовать для выделения клеток.
Как мы это делаем (технологии сохранения МСК и ткани пупочного канатика)
Получите бесплатную консультацию специалиста
Сколько это стоит?
Уважаемые Будущие Родители!
Вот уже более 20 лет Банк пуповинной крови «КриоЦентр» оказывает квалифицированные медицинские услуги по криогенному хранению клеток пуповинной крови. Более 25000 наших соотечественников доверили нам хранить самое ценное – клеточную биологическую страховку своих детей. Но КриоЦентр – не просто банк пуповинной крови – совместно со специалистами различных областей медицины мы занимаемся научным поиском, организуем и проводим клинические исследования, разрабатываем и успешно внедряем новейшие технологии лечения – клеточную терапию.
Сегодня мы рады сообщить, что после успешного завершения всех необходимых исследований и подготовительных работ КриоЦентр готов предоставить Вам новую биомедицинскую услугу: криогенное хранение ткани пупочного канатика и выделенных из нее мезенхимальных стромальных (стволовых) клеток (далее – МСК).
О том, что такое МСК, каковы реалии и перспективы их применения в медицине, Вы узнаете из этой публикации.
МЕЗЕНХИМАЛЬНЫЕ СТВОЛОВЫЕ КЛЕТКИ:
новая эра регенеративной медицины
С момента открытия Александром Яковлевичем Фриденштейном и соавторами в начале 1970-х годов костномозговых «колониеобразующих единиц фибробластов» (КОЕ-ф), эта уникальная клеточная разновидность успела сменить несколько имен. До недавнего времени, наибольшей популярностью среди биологов и клеточных терапевтов пользовался термин «мезенхимальные стволовые клетки» (МСК), предложенный Арнольдом Каплан (Arnold Caplan) в 1990-е годы. Еще через 15 лет по инициативе Международного общества по клеточной терапии (ISCT – International Society for Cellular Therapy) на смену им пришли «мультипотентные мезенхимальные стромальные клетки», сохранившие привычную аббревиатуру МСК.
Все три термина подразумевают популяцию клеток, способных расти в прикрепленном состоянии и дифференцироваться (созревать, приобретать свойства) в экспериментальных условиях, по крайней мере, в трех направлениях: остеогенном, адипогенном и хондрогенном, т.е. давать начало клеткам костной, жировой и хрящевой ткани. В последние годы появились работы, доказывающие способность МСК участвовать в формировании и других типов клеток нашего организма: мышечных, эндотелиальных (выстилающих внутреннюю поверхность кровеносных сосудов), кардиомиоцитов (клеток сердца), гепатоцитов (клеток печени) и даже нейронов.
Традиционные и экзотические источники МСК
Основным источником МСК, как для экспериментальных, так и для клинических исследований, исторически является костный мозг. Однако, лишь от 0,001 до 0,01 % всех клеток, присутствующих в аспирате костного мозга, способны прикрепляться к пластику и давать клональный рост фибробластоподобных элементов. Помимо костного мозга, то или иное количество МСК содержится практически во всех когда-либо исследованных тканях человеческого организма: жировой ткани, амниотической (околоплодной) жидкости, коже, периферической и пуповинной крови, и даже в менструальной крови и пульпе выпавших молочных зубов. Однако выделение и успешное размножение МСК из большинства подобных экзотических источников, как правило, затруднены в связи с методическими сложностями либо с крайне низким содержанием искомых клеток.
Поистине непревзойденным источником МСК являются ткани последа – пуповина и плацента.
Пуповина – уникальный источник МСК
На протяжении всей беременности два организма – мать и плод – соединены пуповиной: похожим на веревку (англ. – umbilical cord – пупочный канатик) образованием диаметром до одного и длиной до 50 сантиметров. Пуповина содержит три кровеносных сосуда, входящих в систему кровообращения плода (две артерии и одну вену), заключенных в желеобразное внеклеточное вещество (Вартонов гель), покрытое снаружи плотной оболочкой. По имеющимся литературным данным все «компартменты» пуповины буквально «нашпигованы» МСК.
Поперечный срез пупочного канатика человека.
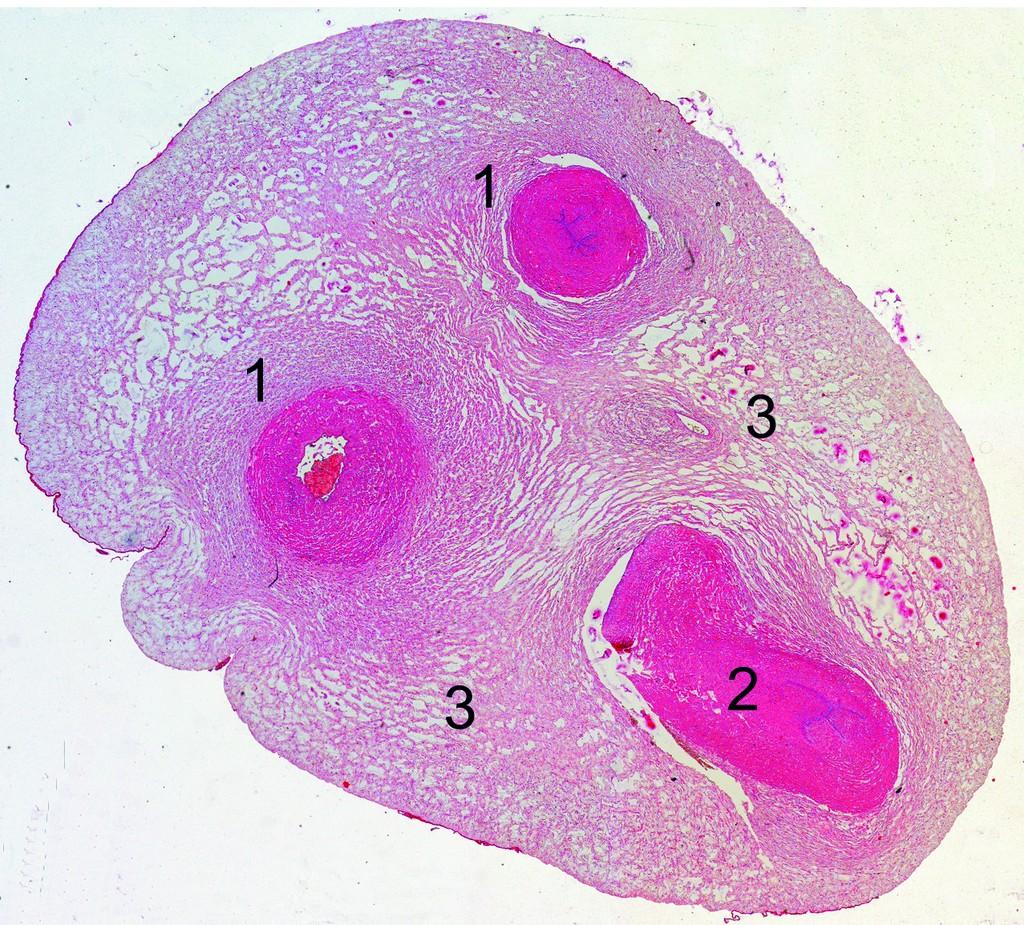 1 – пупочная артерия, 2 – пупочная вена, 3 – Вартонов гель.
1 – пупочная артерия, 2 – пупочная вена, 3 – Вартонов гель.
(Фото любезно предоставлено И.Арутюнян).
По сравнению с клетками взрослого организма МСК пуповины обладают наивысшим пролиферативным потенциалом (способностью к размножению) и биологической активностью, что делает их одним из главных кандидатов на использование в регенеративной медицине и клеточной терапии. Эти клетки могут использовать все три известных механизма репарации: непосредственное превращение в требуемый тип клеток, паракринный и иммуномодулирующий (см. ниже). И хотя МСК пупочного канатика не столь универсальны, как эмбриональные или индуцированные плюрипотентные стволовые клетки, у них есть еще одно неоспоримое преимущество – отсутствие способности к озлокачествлению и формированию тератом в экспериментальных условиях. К тому же, как и в случае клеток пуповинной крови, их получение не вызывает каких-либо этических, религиозных, медицинских или иных проблем, а сама заготовка ткани пупочного канатика проводится уже после рождения ребенка и не несет никаких рисков для него самого или его матери.
Выделение и культивирование МСК пупочного канатика
Поскольку содержание МСК в тканях (в т.ч. пуповине) обычно не превышает долей процента, дальнейшая работа с ними подразумевает необходимость дополнительного размножения в условиях in vitro. Для этого предложены десятки протоколов, основанных на использовании распространенных коммерческих синтетических сред с добавлением сыворотки крови или коктейлей ростовых факторов. Использование процедуры культивирования клеток позволяет в относительно короткие сроки (недели – месяцы) нарастить их число до необходимого (сотни миллионов) для клинического применения.
Мезенхимальные стромальные и эпителиальные стволовые клетки амниона
Амнион (также известный как "амниотическая оболочка") — это самый внутренний слой плаценты, образующий оболочку плацентарного мешка.
Внедренные специалистами КриоЦентра методики позволяют сохранить два вида биологических материалов, получаемых из амниона:
- выделенные мезенхимальные стромальные стволовые клетки, которые при необходимости можно дополнительно размножать для последующего использования;
- собственно ткань амниона как дополнительный источник МСК и с целью последующего выделения и культивирования другой популяции стволовых клеток — эпителиальных.
К настоящему времени исследования показали, что стволовые клетки амниона, как эпителиальные, так и мезенхимальные способны дифференцироваться в адипоциты (жировая ткань), костные, нервные клетки, кардиомиоциты, клетки скелетных мышц, гепатоциты (печень), эндотелиальные клетки (сосуды), клетки почек и сетчатки.
Применение в регенеративной медицине
Исследования показали, что аMCК выделяют целый ряд факторов роста, усиливающих пролиферацию, уменьшающих воспаление и контролирующих различные процессы, необходимые для заживления повреждений. Иммуносупрессивные свойства и способность аMCК секретировать ангиогенные факторы (способствуют росту кровеносных сосудов) делают их важнейшим инструментом для лечения сердечно-сосудистых заболеваний, таких как критическая ишемия конечностей и инфаркт миокарда. Способность стволовых клеток дифференцироваться в функциональные клетки-предшественники нейронов позволяет использовать аMCК при лечении черепно-мозговой травмы и повреждения спинного мозга. Эффективность АМСК также изучают на моделях диабета.
Эпителиальные стволовые клетки исследуют при болезни Паркинсона, инсульте, фиброзе и циррозе печени, бронхопульмональной дисплазии недоношенных новорожденных.
Обе популяции клеток применяют (в качестве цельной ткани и выделенных из нее клеток) в офтальмологии, дерматологии, гинекологии, лечении синдрома запястного канала, свищей, медикаментозно вызванном остеонекрозе челюсти (осложнение химиотерапии).
Синтетическая и секреторная активность МСК
В силу анатомического расположения и многочисленных выполняемых ими функций, МСК синтезируют и секретируют целый ряд компонентом внеклеточного матрикса (фибронектин, коллаген, ламинин, протеогликаны) и растворимых соединений. МСК продуцируют ростовые факторы, цитокины и хемокины, непосредственно участвующие в поддержании нормального функционирования органов и тканей, в том числе интерлейкины (ИЛ) -1α и -1β, ИЛ-6, ИЛ-7, ИЛ-8, ИЛ-11, ИЛ-14 и ИЛ-15, макрофагальный (m-csf) и гранулоцитарно-макрофагальный (GM-CSF) ростовые факторы, фактор стволовых клеток (SCF), тромбопоэтин и фактор роста гепатоцитов (HGF). Некоторые из этих соединений продуцируются спонтанно, другие – в ответ на активацию. Вместе и по отдельности эти факторы участвуют как в поддержании нормального гомеостаза организма, так и в процессах регенерации (восстановления) поврежденных органов и тканей.
Иммуномодулирующие свойства МСК
Способность МСК оказывать анти-пролиферативные, иммуномодулирующие и противовоспалительные эффекты при различных патологических состояниях в последнее время привлекает все больше внимания. Это связано с тем, что сами МСК являются слабо иммуногенными и практически не вызывают отторжения организмом реципиента. Отсутствие на их поверхности ряда молекул дает основания для использования в терапевтических целях аллогенных (донорских) клеток. При этом иммуносупрессивные свойства МСК определяются как плеядой продуцируемых ими растворимых факторов («паракринный» механизм действия), так и непосредственными межклеточными контактами. И те и другие способны кардинально влиять на течение физиологических и патологических процессов, изменяя свойства клеточного микроокружения с про- на противовоспалительные.
Биологические маркеры МСК
В настоящее время не существует какого-либо уникального маркера, позволяющего однозначно сказать о принадлежности клеток к категории МСК. Как и любые другие клетки организма, МСК несут на своей поверхности сотни белков, так или иначе связанных с выполнением возложенных на них функций. Среди них и молекулы адгезии, ответственные за межклеточные взаимодействия, и рецепторы биологически активных веществ (цитокинов и факторов роста), и белки, опосредующие распознавание «свой-чужой», т.е. работу иммунной системы, и многие другие. Большинство их них объединено под названием «кластер дифференцировки» (cluster of differentiation, CD) в специальную классификацию.
По рекомендациям Международного общества по клеточной терапии к обязательным для МСК маркерам относятся такие как CD90, CD73 и CD105, а также антиген лейкоцитов человека 1-го типа (Human Leukocyte Antigen – 1, HLA-I). Помимо них, МСК несут на поверхности CD13, CD29 и CD44, CD54, CD71 и (реже) CD106. Одновременно, МСК не содержат признанных маркеров клеток крови, кроветворных или эндотелиальных клеток-предшественников, такие как CD34, CD45, CD133 и HLA-DR. Подобный «фенотип» МСК обычно и используется при составлении паспорта на клеточный продукт, предназначенный для научных исследований или клинического применения.
Терапевтический потенциал МСК
Многие из характеристик МСК, в том числе, способность к дифференцировке в различные клеточные типы in vitro и in vivo, делают их весьма привлекательными с точки зрения возможного использования для клеточной терапии широкого спектра приобретенных и наследственных заболеваний. Как при системном (внутривенном, внутриартериальном), так и при локальном (непосредственно в ткань-мишень) введении, МСК обладают способностью к «хоумингу» (от англ. home – дом) и длительному существованию в различных органах и тканях реципиента. Кроме этого, при введении в системный кровоток клетки способны целенаправленно мигрировать в участки повреждения и участвовать в их восстановлении, что убедительно доказано в моделях костных переломов, ишемии мозга и инфаркта миокарда. Имеются указания на попытки применения МСК и для восстановления дефектов суставного хряща.
В последовавших за экспериментом клинических исследованиях, проведенных на ограниченном числе пациентов, была доказана возможность использования МСК или их смеси с кроветворными клетками-предшественниками при ишемии конечностей и миокарда, а также при незаживающих хронических повреждениях кожи. Обнадеживающие результаты достигнуты при лечении неврологических и кардиологических заболеваний. Проведенные исследования показали, что трансплантация МСК может оказаться эффективной при ишемическом инсульте, травматических повреждениях головного и спинного мозга, инфаркте миокарда. Еще одним примером успешного системного введения МСК могут служить работы, подтверждающие ускоренное восстановление кроветворения при трансплантации кроветворных стволовых клеток и положительный эффект при лечении тяжелых форм острой и хронической болезни «трансплантат-против-хозяина (РТПХ), что связано с выраженными «иммуномодулирующими» свойствами МСК. Имеются сообщения об успешном использовании МСК при лечении заболеваний и других органов: легких, мышц и почек.
Неполный перечень проводящихся в настоящее время клинических исследований с использованием МСК пупочного канатика приведен в таблице.
Криогенное хранение МСК
Как и большинство других типов клеток человека, МСК пупочного канатика могут на протяжении десятилетий сохранять свои биологические свойства в криогенных условиях (в жидком азоте). Впоследствии, клетки могут быть успешно разморожены без потери качества и использованы (в зависимости от имеющегося количества) либо для клинического применения, либо для последующего размножения с той же целью.
Заключение
Успехи, достигнутые в изучении биологии МСК человека in vitro и на экспериментальных моделях in vivo, не могли не привлечь к себе внимание практических врачей. Количество клинических исследований, официально объявляемых в разных странах мира, исчисляется сотнями и неуклонно возрастает, равно как и число отчетов, свидетельствующих об эффективности клеточной терапии при различных патологических состояниях. С открытием и успешным выделением МСК из различных пост-эмбриональных тканей, включая ткань пупочного канатика, началась новая эра клеточной терапии. Хочется верить, что уже в обозримом будущем и эти клетки займут достойное место в арсенале средств практической медицины и выведут ее на принципиально новый уровень развития – уровень регенеративной медицины.
